Ученые из Пущино узнали, из-за чего происходят судороги при эпилепсии
Сотрудники Института теоретической и экспериментальной биофизики РАН г.Пущино, совместно с зарубежными коллегами исследовали механизмы развития нарушений работы мышечного аппарата при хронической обструктивной болезни легких. Результаты этой работы опубликованы в журнале Biochimica et Biophysica Acta (импакт-фактор 5.083).
Хроническая обструктивная болезнь легких (ХОБЛ) — это болезнь, для которой характерно устойчивое нарушение движения воздушного потока из легких. Это угрожающее жизни заболевание, которое препятствует нормальному дыханию. Лечение позволяет замедлить течение этой болезни, но до сих пор она остаётся неизлечимой. По данным ВОЗ в 2012 году от ХОБЛ умерло более 3 миллионов человек, что составило почти 6% всех случаев смерти в мире в этом году. Самыми распространенными симптомами ХОБЛ являются одышка и хронический кашель. По мере постепенного развития болезни может значительно затрудняться ежедневная физическая активность, даже такая, как подъем на несколько ступеней по лестнице. Факторами риска для развития этого заболевания является табачный дым, загрязненный воздух, хронические заболевания органов дыхания. По этой причине ни один житель нашей планеты не застрахован от ХОБЛ.
Международная группа исследователей, включающая ученых ИТЭБ РАН, Альпийского университетского центра в Гренобле (Франция), университета Барселоны (Испания) и клиники Мейо (США) определили новый фактор, который вызывает нарушения работы мышечного аппарата у больных с ХОБЛ. Этот фактор связан с ограничением подвижности энергетических субстратов между центрами их производства и потребления внутри клетки. Таким энергетическим субстратом является АТФ (аденозинтрифосфат) - универсальным «топливом»для всех энергозависимых жизненно важных внутриклеточных процессов, в том числе и для мышечного сокращения.
У больных хронической обструктивной болезнью легких даже при небольших физических нагрузках возникает серьезный дискомфорт. Казалось бы, что уровень АТФ, необходимый для работы мышц при таком состоянии должен быть снижен. Однако, у больных с ХОБЛ, даже при недостаточном сокращении мышц, не нарушена способность к воспроизводству АТФ, а также отмечен избыточный уровень этого источника энергии. Для того чтобы объяснить этот парадокс, авторы использовали представление о том, что внутриклеточный объем представляет собой разделенное на отдельные части (компартменты) пространство. По причине этого разделения внутри клетки не происходит хорошего перемешивания компонентов, т.е. ограничивается их диффузия. Ученые использовали данные здоровых людей и пациентов с ХОБЛ для построения пространственно-временного распределения АТФ внутри саркомера – базовой сократительной единицы. Поскольку в настоящее время не существует экспериментальных методов прямой оценки распределения АТФ внутри саркомера, авторы применили глубокий компьютеризованный математический анализ процессов диффузии, утилизации и воспроизводства АТФ внутри и вблизи мышечного саркомера четырехглавой мышцы бедра, во время проведения клинических стресс-тестов.
- Микроанатомическое строение саркомеров подразумевает наличие молекулярных барьеров, которые ограничеваюте диффузию АТФ от мест его производства в клетке к центрам его утилизации внутри саркомеров. Именно эти диффузионные барьеры провоцируют появление микроучастков истощения АТФ в саркомерах пациентов с ХОБЛ, несмотря на то, что средний уровень АТФ в клетке остается высоким и не отличается от уровня здоровых людей, - рассказывает один из авторов этой работы, научный сотрудник Сектора регуляции ионных каналов ИТЭБ РАН Алексей Алексеев, - Появление таких зон истощения АТФ приводит к отсутствию расслабления соответствующих участков сокращенных мышц. Из-за этого падает сила сокращения, а также могут возникать болевые ощущения, типичные для больных ХОБЛ, связанные с микроразрывами мышечной ткани, что в свою очередь, может инициировать патологические процессы, ведущие к мышечным заболеваниям. Ограниченная диффузия АТФ внутри саркомеров при несоответствии между кислородо-зависимой скоростью воспроизводства АТФ и скорости его потребления, даже при пониженном уровне физической нагрузки представляет собой ранее неизвестный риск-фактор ограниченной работоспособности опорно-двигательной системы у больных с ХОБЛ.
Авторы исследования полагают, что ограниченная диффузия энергетических субстратов, включая АТФ, может вносить вклад в развитие и других энерго-дефицитных заболеваний, связанных с мышечной миопатией, ишемической болезнью сердца и сердечной недостаточностью.
В целом, данное исследование является одним из первых применений концепции внутриклеточной компартментации для объяснений симптоматики заболеваний человека.
Источник: Alekseev AE, Guzun R, Reyes S, Pison C, Schlattner U, Selivanov VA, Cascante M., Restrictions in ATP diffusion within sarcomeres can provoke ATP-depleted zones impairing exercise capacity in chronic obstructive pulmonary disease. Biochim Biophys Acta. 2016 Oct; 1860(10):2269-78.
http://www.sciencedirect.com/science/article/pii/S0304416516301234
Рисунок, изображающий строение саркомера предоставлен авторами работы.
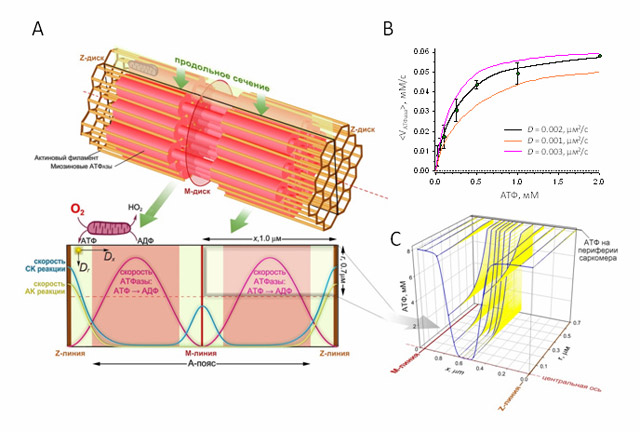
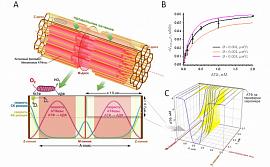
Рисунок. Структура саркомера и внутренние диффузионные ограничения.
А: схема, иллюстрирующая локализацию миозиноновый АТФазы, фосфотрансферных реакций, катализируемых креатин - (СК) и аденилат - (АК) киназами внутри саркомера, и условное положение митохондрий, обеспечивающих аэробный ре-синтез АТФ на периферии саркомера. Маркированная вставка, длиной х = 1,0 μм и радиусом r = 0,7 μм, представляет четверть пространства саркомера, для которого представлено пространственное распределение АТФ. Dr и Dx обозначают радиальную и продольную диффузию АТФ внутри структуры саркомера, включающей актиновые филаменты и центры миозиновой АТФазы.
В: экспериментально измеренные скорости АТФазной реакции () в образцах биопсии контрольной группы и ХОБЛ пациентов и наилучшее значение кажущегося диффузионного коэффициента (D = 0,002 μм2/с). Для сравнения – диффузионный коэффициент свободной диффузии АТФ в цитозоле составляет около 150 μм2/с.
С: Распределение АТФ в четверти пространства саркомера от Z-линии к М-линии и от периферии к центральной оси, при вычисленных коеффициентах диффузии. Концентрация АТФ вне саркомера 8,2 мМ.
Материал подготовила пресс-секретарь ИТЭБ РАН Татьяна Перевязова iteb-press@yandex.ru